8 Zustandsgleichung für ideale Gase
Luft dehnt sich aus, wenn sie warm wird und sie zieht sich zusammen, wenn sie kalt wird. Das liegt daran, dass sich warme Luftmoleküle schneller bewegen als kalte. Dann stoßen sie sich auch stärker voneiander ab, wenn sie zusammenprallen.
Das wird durch die Zustandsgleichung für ideale Gase beschrieben:

Dabei ist
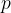 der Druck des Gases
der Druck des Gases
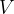 das Volumen des Gases
das Volumen des Gases
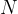 die Anzahl der Gasteilchen
die Anzahl der Gasteilchen
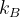 die Boltzmann-Konstante
die Boltzmann-Konstante 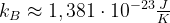
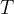 die Temperatur in Kelvin (Temperatureinheit Kelvin siehe hier)
die Temperatur in Kelvin (Temperatureinheit Kelvin siehe hier)
Da aber die Moleküle eines Gases nicht so einfach zu zählen sind, gibt es auch eine Variante dieser Gleichung, die mit der Masse eines Gases formuliert wird an Stelle der Anzahl der Gasmoleküle:

Dabei ist
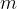 die Masse ds Gases und
die Masse ds Gases und
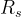 die inidividuelle - man sgt auch spezifische - Gaskonstante eines Gases
die inidividuelle - man sgt auch spezifische - Gaskonstante eines Gases
Trockene Luft hat zum Beispiel eine spezifische Gaskonstante von 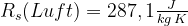
Die wichtige Folgen dieser Gleichung
Wenn wir Experimente mit Luft machen, dann sind die Masse des Gases und die Gaskonstante konstant. Gaskonstanten kann man in Tabellenbüchern finden.
Wenn der Druck gleich bleibt
Wenn wir zum Beispiel ein Experiment in offenen Gefäßen machen, dann kann der Luftdruck sich jederzeit ausgleichen. Der Druck ist also immer gleich. Dann ist das Volumen eines Gases proportional zu der Temperatur in Kelvin.
Das heißt es gilt

Das heißt in Worten: Wenn die Temperatur (in Kelvin) um einen bestimmten Prozentsatz steigt oder fällt, dann steigt oder fällt das Volumen um genau so viel Prozent.
Beipiel: Über eine kalte Ein-Liter-Flasche wird ein Luftballon gestülpt. Wenn die Flasche nun von 20°C auf 40°C erwärmt wird, dann dehnt sich der Luftballon aus.
Bei diesem Experiment wirkt der Luftdruck des Raumes auf den Luftballon und auf die Flasche. Der Druck bleibt daher immer der gleiche.
Um wie viel wächst dann das Volumen des Gases?
- Zuerst müssen die Temperaturen in Kelvin umgerechnet werden: 20°C = 293,15K und 40°C = 313,15K
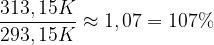
Die Temperatur ist also um 7% gewachsen. Dann wächst das Volumen der Luft in der Flasche auch um 7%:
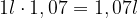
0,07 l Luft sammeln sich also im Luftballon
Was muss ich wissen?
- Wenn Gase warm werden, dann dehnen sie sich aus
- Wenn Gase kalt werden, dann ziehen sie sich zusammen
- Ich weiß wie man eine Temperatur in Kelvin umrechnet
- Wenn der Druck bei einem Experiment gleich bleibt, dann steigt bzw. fällt das Volumen um genau so viel Prozent, wie die Temperatur in Kelvin
Backlinks:
2 Physikbücher:Naturwissenschaften für die FSP
